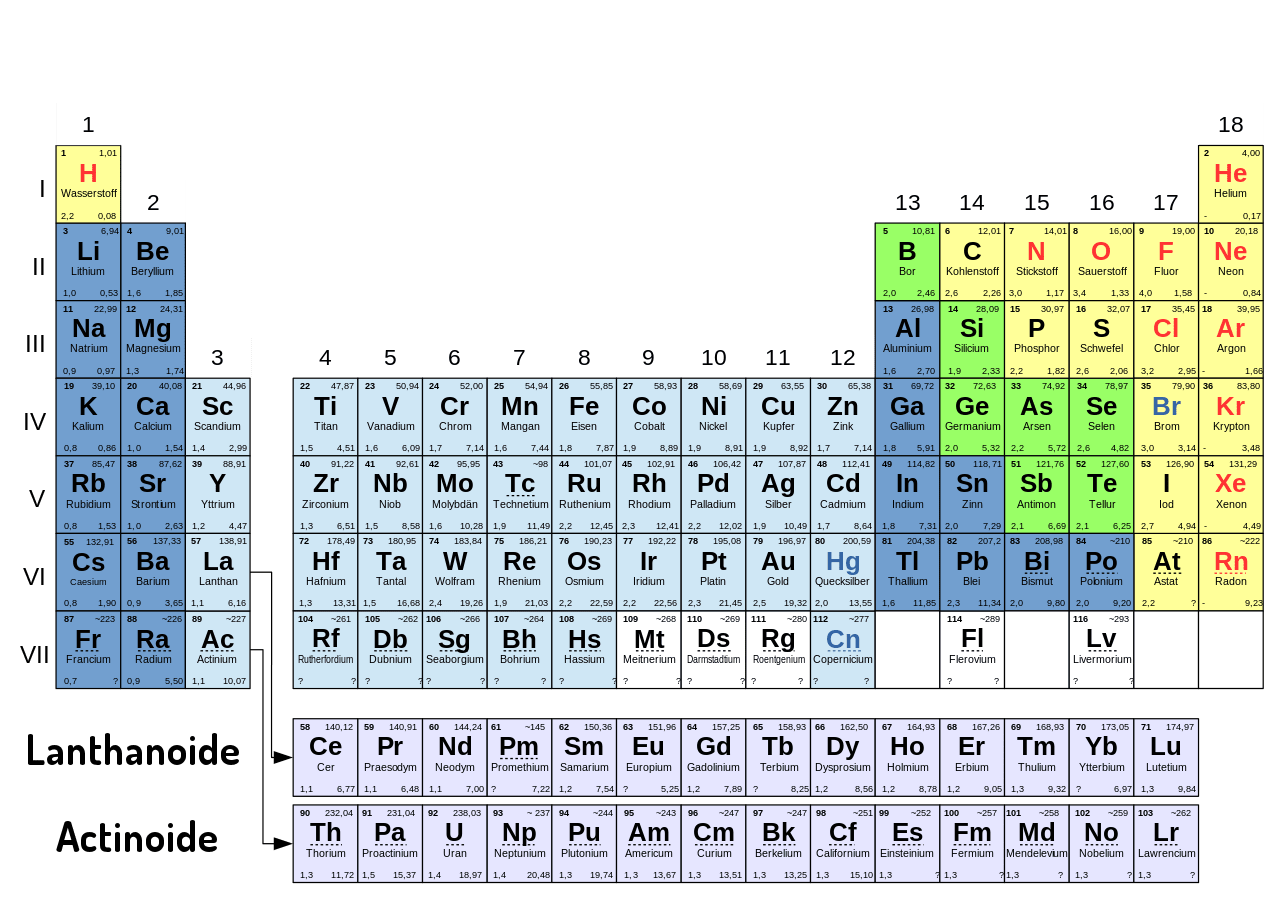
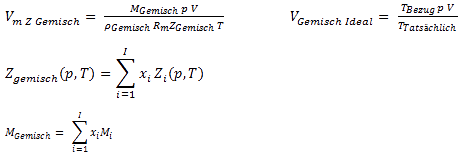p = Druck R* = universale Gaskonstante n = Stoffmenge V = Volumen R = R*/M spez. Gaskontante T = absolute Temperatur M = molare Masse m = Masse - PDF Kostenfreier Download

n = V Lsg m n l mol Grundwissen 9. Klasse Chemie (NTG) Analytische Chemie Stoffmenge n Molare Masse M Molares Volumen V M Stoffmengenkonzentration c - PDF Free Download
Partielle molare Größen und GIBBS-DUHEM Beziehung - Wie verändert sich eine Mischung bei Zugabe von 1 mol Komponente A? - TIB AV-Portal
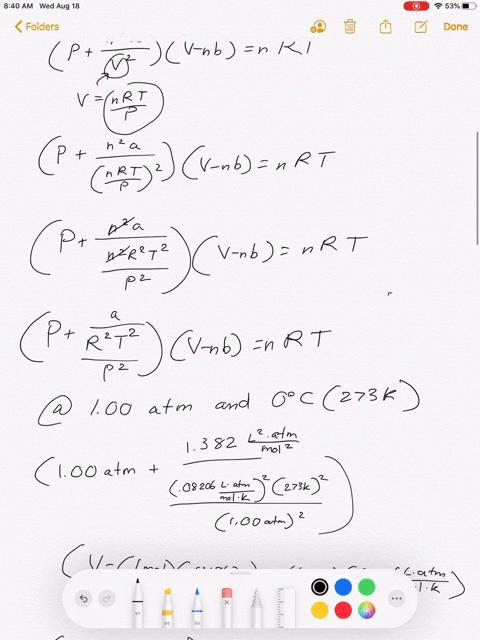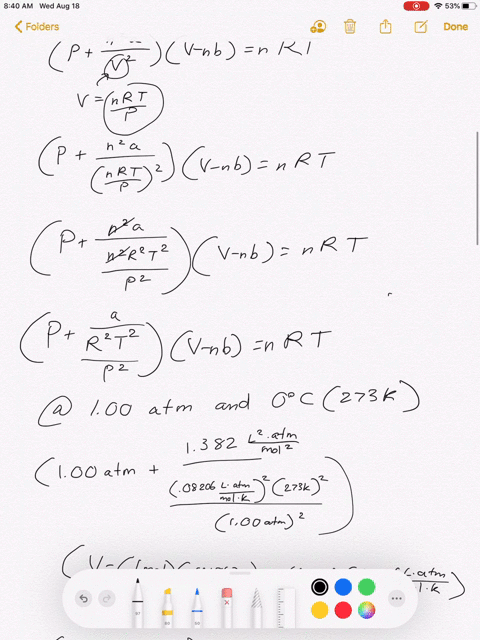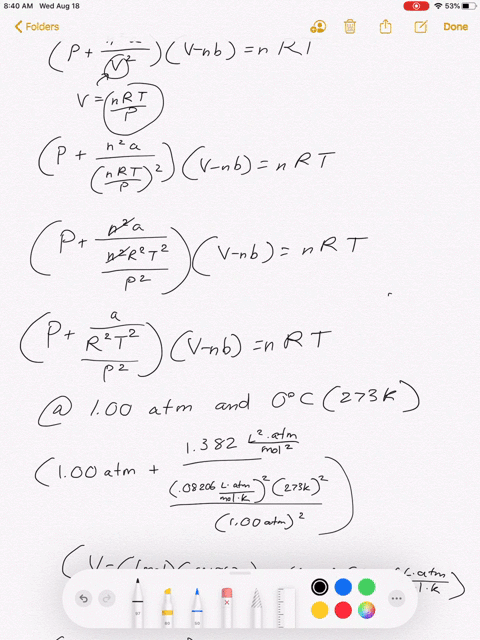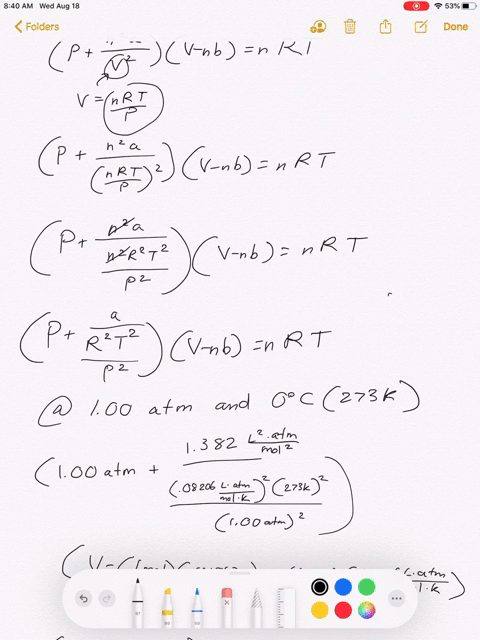





![Molare Masse berechnen · Formel + Berechnung · [mit Video] Molare Masse berechnen · Formel + Berechnung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/10/WP_Molare-Masse_pse-1-1024x576.jpg)

![Feuchte Luft – Zustandsgrößen | einfach erklärt! · [mit Video] Feuchte Luft – Zustandsgrößen | einfach erklärt! · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2018/12/pic1_SEO-1-1024x576.jpg)